
Descifrado el mecanismo de una mutación que altera los niveles de cloro en la retina
El equipo de investigación de IMO Grupo Miranza ha dado un paso importante en el conocimiento del mecanismo que hay detrás de una de las distrofias maculares más prevalentes, la enfermedad de Best. En el transcurso de un estudio de Fundación IMO sobre el efecto de las mutaciones genéticas de siete pacientes con distrofias de retina (Stargardt, retinosis pigmentaria, acromatopsia y enfermedad de Best), los investigadores han dado con este importante descubrimiento, publicado recientemente en el International Journal of Molecular Science.
A los pacientes incluidos en el estudio, iniciado hace cinco años, se les hizo una biopsia de piel para, a partir de ella, inducir células madre, que, ahora, y mediante técnicas de diferenciación celular, han convertido en células de retina para estudiar en ellas por qué la mutación genética de cada paciente causa su distrofia retiniana.
Un avance en distrofias maculares con valor añadido
En esta indagación, los investigadores han estudiado, entre otras, una mutación particular, no descrita en otras familias, en una paciente con la enfermedad de Best, segunda distrofia macular más prevalente, que suele aparecer en la infancia o adolescencia y que afecta a la mácula y disminuye bruscamente la agudeza visual. El gen implicado en la enfermedad es el gen BEST1, del que se han descrito más de 350 mutaciones, pero ninguna, hasta ahora, como la que presenta esta paciente. Asimismo, el hecho de que en este caso la investigación se haya realizado a partir de células de la propia paciente, en lugar de en modelos in vitro, como en otros estudios, aporta al hallazgo un valor añadido.
Según la Dra. Esther Pomares, responsable del Departamento de Genética de IMO Grupo Miranza, “hemos podido descifrar y describir el mecanismo específico que desencadena esta mutación, alterando la entrada de cloro en las células del epitelio pigmentario de la retina, que son las que quedan afectadas por esta enfermedad”.
Concretamente, los genetistas implicados en el estudio de Fundación IMO, han analizado las consecuencias de la alteración del aminoácido 77, donde la paciente tiene la mutación. Este aminoácido está situado en el cuello del canal que regula la apertura y cierre del mismo y la entrada de cloro en las células de la retina. Los investigadores han podido descifrar que dicha alteración deja el canal abierto, y no cerrado, como se ha descrito en la mayoría de casos de esta patología, estudiados previamente.
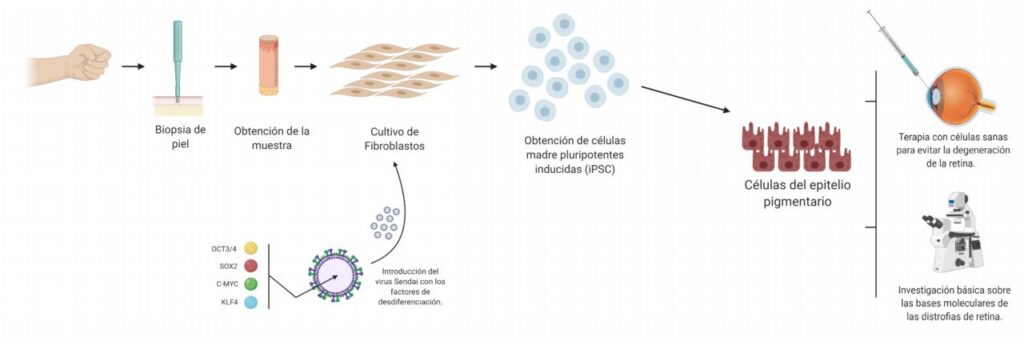
Posibilidad de terapias específicas de retina para cada paciente
Según el Dr. Arnau Navinés, investigador que ha liderado el estudio, “un mejor conocimiento del mecanismo de la enfermedad, abre la puerta al diseño de terapias específicas para cada paciente”. En este caso, por ejemplo, “nos plantearíamos realizar una terapia génica de bloqueo o adición, anulando la proteína mutante o añadiendo bestrofinas (proteína del gen BEST1), para restaurar los niveles adecuados de esta proteína. De esta forma, se evitaría la muerte celular y se detendría la progresión de la enfermedad, regulando, así mismo, los niveles de cloro de la retina”.